| Språk : |
|
| Encyclopedia gemenskap |Encyclopedia Svar |Submit fråga |Ordförråd Kunskap |Överför kunskap |
Irene ekvation |
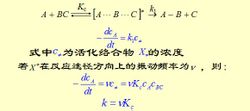  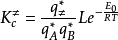 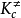 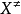 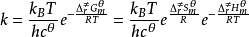 |
|
Irene ekvation [1] Transition state teori antaganden: Reaktantmolekyler kolliderar med varandra när konfigurationen av övergångstillståndet av reaktionsprodukten sker.De reaktanter och aktiverade komplex termodynamisk jämvikt kan nås genom bearbetning; Omvandlingen till det aktiverade komplexet är reaktionsprodukten av det hastighetsbestämmande steget. Aktiverat komplex molekyl längs reaktionen koordinaten rörelsen av produkten omvandlades till rörelsen med andra separation. Enligt statistisk termodynamik jämviktskonstant för ekvationen, får vi: Detta beräknas av övergångstillståndet teorin bimolekylär hastighetskonstant av de grundläggande ekvationer, som ibland kallas Irene (Eyring H) ekvation I princip, så länge vet om strukturen hos molekylen kan beräknas enligt formeln hastighetskonstanten k, utan att behöva göra kinetik. Irene termodynamiska ekvationen uttryck Nämligen bimolekylära reaktioner Irene termodynamiska ekvationen uttryck. Irene ekvation kan användas för enstaka molekyl eller tre-molekyl reaktioner, och reaktionslösningen, men något annorlunda form med denna stil. Fördelen med övergångstillståndet teori 1 skildrar livfullt hur elementära reaktioner process förklarar innebörden av reaktionen genom; (2) kan i princip från den atomära strukturen av de spektrala data och beräknade potentiell energi ytreaktion hastighetskonstant k, är det också kallas den absoluta teori reaktionshastigheten; 3 om Arrhenius pre-exponentiell faktor och den teoretiska förklaringen, att det avsåg med entropi för aktivering; 4 illustrerar tydligt varför du behöver aktiveringsenergin för reaktionen, och reaktionen följer principen om minsta energi. : Transition state teori brister En jämvikt antagande och införandet av hastighetsbestämmande steget hypotesen uppfyller inte alla de experimentella fakta; 2 par komplexa polyatomära reaktioner har svårt att dra potentiell energi yta, så att tillämpningen av teorin med vissa begränsningar. Tre par av komplexa polyatomära reaktioner, aktiverad komplex konfiguration av fortfarande osäker. : |
| Användare Omdöme |
|
Inga kommentarer |